Modernste Diagnostik von Tumorgewebeproben

Die mittlere Ischämiezeit, d. h. die ohne dauerhaften Gewebeschaden tolerierte Zeitspanne bei der Gewebeentnahme, beträgt weniger als zehn Minuten.
Um ein möglichst umfassendes Bild der individuellen Tumorbiologie und potenzieller Angriffspunkte zu erhalten sowie wirksame Medikamente zu identifizieren, kombinieren wir verschiedene innovative Untersuchungsmethoden.
Genetische Veränderungen
Sequenzierung der Tumor-DNA zum Nachweis krebsrelevanter Veränderungen in den Genen, die ursächlich für das Krebsgeschehen verantwortlich sind.
Krebsrelevante Veränderungen der Proteine
Nachweis bestimmter Rezeptoren auf der Zelloberfläche, veränderter Eigenschaften des Immunsystems und Untersuchung der Fähigkeit der Zellen, entstandene Schäden an der DNA zu korrigieren, mit Hilfe automatischer Gewebefärbeverfahren.
Krebsrelevante Veränderungen in der zellulären Kommunikation
Bestimmung der Aktivität von Eiweißmolekülen, die für die Regulation des Krebswachstums von Bedeutung sind, unter Verwendung hochempfindlicher Messmethoden.
Die Grundlage für zuverlässige Ergebnisse unserer Analytik ist eine hohe Qualität der zu untersuchenden Gewebeproben. Wir verwenden daher die von Indivumed entwickelten standardisierten Prozesse zur Gewebeentnahme. Speziell ausgebildete Mitarbeiter stellen im Operationssaal sicher, dass das entnommene Gewebe in weniger als zehn Minuten aufbereitet und fixiert wird, da nur dann das molekulare und biologische Tumorprofil so erhalten bleibt, wie es im menschlichen Körper vorkommt.
Diagnostisches Konzept
Unser Ziel ist es, anhand von Gewebeproben das molekulare Profil eines Tumors unabhängig von seiner Lokalisation zu analysieren. Nur so lassen sich umfassend therapeutische Angriffspunkte identifizieren, die Krebspatienten im fortgeschrittenen Stadium IV weitere Behandlungsoptionen eröffnen können.
Um ein möglichst vollständiges Bild des Tumors zu erhalten, setzen wir modernste Technologien für die Analytik ein. Wir untersuchen nicht nur das Auftreten von Mutationen in sogenannten Hotspot-Regionen von 50 Onkogenen und Tumorsuppressorgenen, sondern auch die Expression von Proteinen innerhalb der Zelle und auf der Zelloberfläche sowie die Phosphorylierung/Aktivierung von Signalproteinen krebsrelevanter Signalwege.
Die Grundlage für zuverlässige Ergebnisse der Analytik ist eine hohe Qualität der zu untersuchenden Gewebe. Verschiedenste Studien haben gezeigt, dass der standardisierten und schnellen Gewebeprozessierung nach Gewebeentnahme eine entscheidende Bedeutung für die Aussagekraft der Proteinanalytik zukommt.
Aus diesem Grund können wir z. B. die Signalweganalytik nur dann durchführen, wenn die Gewebeentnahme nach dem von Indivumed erarbeiteten Standard erfolgt.
Unsere Analyseergebnisse werden anschließend von einem interdisziplinären Team von Ärzten, Pathologen und Wissenschaftlern anhand der klinischen Daten und einer umfangreichen Literaturrecherche bewertet sowie auf die Verfügbarkeit klinischer Studien überprüft. Dabei ziehen wir auch zielgerichtete Wirkstoffe außerhalb der zugelassenen Indikation in Betracht, sofern sie in klinischen Studien in der entsprechenden Tumorentität bereits eine Wirksamkeit gezeigt haben. Der behandelnde Onkologe erhält auf diese Weise wertvolle zusätzliche Informationen für seine Therapieentscheidung.

Facharztinformationen
Die Möglichkeit der Analyse individueller molekularer Tumorprofile von Patienten hat in den letzten Jahren die Grundauffassungen der Onkologie wesentlich verändert und damit die Voraussetzung für personalisierte Krebstherapien geschaffen. Dabei werden mehr und mehr Veränderungen als Tumortreiber identifiziert, die Angriffspunkte für erfolgreiche, zielgerichtete Therapien darstellen.
Um die Komplexität der individuellen Erkrankung auf allen Ebenen zu erfassen, verfolgen wir einen sogenannten Multi-Omics-Ansatz, der das Tumorgeschehen in der gesamten Tumorzelle beleuchtet.
Wir empfehlen unsere forschungsbasierte Analytik für alle Patienten mit fortgeschrittenen, soliden Tumoren, bei denen
- eine wirkungsvolle etablierte Therapie nicht verfügbar ist
- sich die Leitlinientherapie als wirkungslos erwiesen hat
- andere Gründe gegen die Verwendung der üblichen Therapie sprechen
Für die Sequenzierung der Tumor-DNA setzen wir ein Hochdurchsatzsystem ein, das die gleichzeitige Sequenzierung von Millionen einzelner DNA-Fragmente ermöglicht (Next-Generation Sequencing). Damit lassen sich auch kleinste DNA-Mengen – aus kryokonservierten sowie formalinfixierten Gewebeproben – auf relevante Veränderungen untersuchen, die ursächlich für das Krebsgeschehen sind und zugleich einen Hinweis auf die Wirksamkeit von Medikamenten geben. Die Anwendung dieses Verfahrens ermöglicht die Analyse von „Hotspot“-Regionen einer, dem aktuellen Kenntnisstand angepassten, wachsenden Anzahl von Genen.

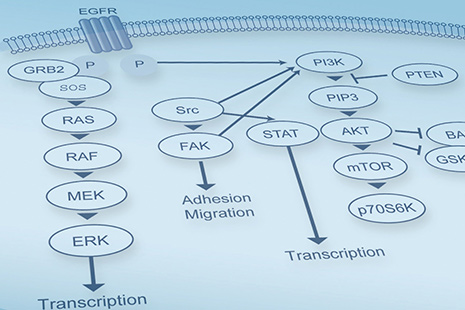
Bei dieser Analytik untersuchen wir die Aktivität (Phosphorylierung) von Signalwegmolekülen sowie fehlregulierte Signalwege im Inneren der Krebszelle, die mögliche Angriffspunkte für Medikamente darstellen. Neben einigen bereits zugelassenen Wirkstoffen, die diese Signalwege blockieren, befinden sich zahlreiche Wirkstoffe in der klinischen Prüfung.
Für die Analyse setzen wir Gewebeproben ein, die umgehend nach der Entnahme kryokonserviert wurden und deren Phosphorylierungsstatus durch sofortige Überführung in flüssigen Stickstoff fixiert wurde. Anhand des prozentualen Anteils phosphoryliert vorliegender Signalproteine können wir so den Aktivierungsstatus des Signalweges ablesen. Zur Interpretation und Bewertung der vorhandenen Ergebnisse setzen wir diese in Bezug zu Daten von Kontrollzellen und Patientenvergleichsgruppen.
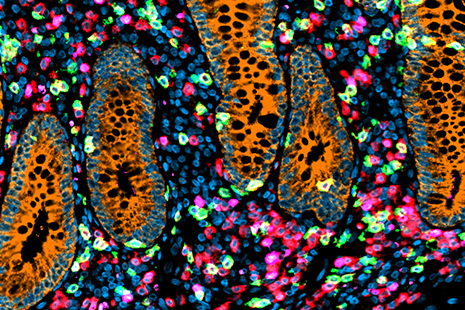
Mit Hilfe von immunhistologischen Analysen (IHC) können wir Rezeptorproteine auf der Zelloberfläche von Tumorzellen nachweisen, die eine Bindungsstelle für Signalmoleküle, Proteine oder Hormone bilden, welche eine Signalübertragung ins Zellinnere auslösen. Sind diese Rezeptoren auf der Zelloberfläche in veränderter Menge vorhanden, kann es zu einer verstärkten Aktivierung oder Inaktivierung von Signalwegen kommen. Damit stellen Rezeptoren einen wichtigen Angriffspunkt für Medikamente dar, die diese z. B. durch spezielle Antikörper gezielt blockieren und damit die fehlregulierte Signalübertragung ins Zellinnere unterbinden.
Weiterhin werden Proteine erfasst, die für veränderte Eigenschaften des Immunsystems und für die Fähigkeit von Zellen, entstandene Schäden an der DNA zu korrigieren, eine Rolle spielen.
Bei unseren Untersuchungen am Tumorgewebe entstehen große Datenmengen, die uns Informationen über die im Tumor bestehenden grundlegenden biologischen Voraussetzungen und Prozesse liefern. Um aus diesen Daten konkrete Empfehlungen für eine wirksame Therapie ableiten zu können, ist eine umfangreiche Analyse unter Einbeziehung und Gewichtung jedes einzelnen Parameters notwendig. Wir verwenden hierzu einen Algorithmus unter Einbeziehung von medizinischen Wissensdatenbanken, veröffentlichter wissenschaftlicher Literatur, deutschen und internationalen medizinischen Leitlinien, den in der Zulassung beschriebenen Anwendungsgebieten und klinischen Studien und erstellen so für den individuellen Tumor eine Interpretation, wie unsere Analyseergebnisse für die Weiterbehandlung genutzt werden könnten.
Ein interdisziplinäres Team von Ärzten, Pathologen und Wissenschaftlern bewertet umfassend alle Ergebnisse unserer integrativen Datenanalyse und überprüft die Verfügbarkeit passender klinischer Studien. Unser Hauptaugenmerk liegt dabei auf den gefundenen molekularen Angriffspunkten und der Identifikation zielgerichteter Wirkstoffe. Dabei werden auch Medikamente außerhalb der zugelassenen Indikation in Betracht gezogen, insbesondere wenn sie in klinischen Studien in der entsprechenden Tumorentität bereits eine Wirksamkeit gezeigt haben. Als behandelnder Onkologe erhalten Sie so mit dem Befundbericht wertvolle zusätzliche Informationen, anhand derer Sie die optimale Therapie auswählen können.

